近日,广东医科大学基础医学院梁峥琰(第一作者)、周军智(通讯作者)等在国际知名期刊《Clinical and Translational Medicine》(中科院1区,Q1, IF=7.9)在线发表了题为“The emerging roles of UFMylation in the modulation of immune responses”的综述论文。

犹素修饰(UFMylation)是2004发现的一种新型类泛素修饰,在真核生物中高度保守(除酵母等真菌)。 犹素系统主要由犹素分子(UFM1),E1激活酶(UBA5),E2结合酶(UFC1),E3连接酶(UFL1),犹素特异性半胱氨酸蛋白酶UFSP1和UFSP2,以及衔接蛋白UFM1结合蛋白1(DDRGK1)和CDK5调节亚基相关蛋白3(C53)组成。成熟的UFM1通过UBA5/UFC1/UFL1三级酶联反应对靶蛋白的赖氨酸残基进行共价修饰。UFM1完成了对底物分子的修饰后,被UFSP1和UFSP2从底物上释放出来,进入下一轮循环。犹素系统在生物体的发育和稳态维持中发挥关键作用,其功能失调与多种疾病的发生发展相关。近年来,越来越多研究揭示犹素系统直接或间接调控多种免疫过程。该综述总结了犹素系统调控免疫应答的机制和功能,提出了犹素修饰系统的潜在临床应用前景,有助于进一步深入了解犹素系统的生物学意义,为人类疾病诊治开发潜在靶点提供理论基础。
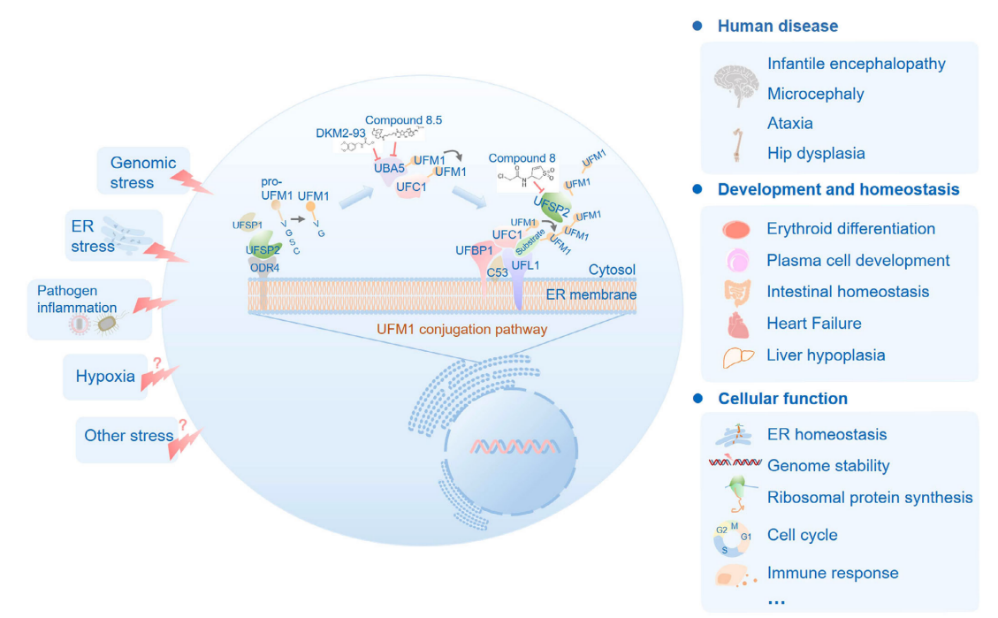
图1.犹素系统组成和功能
UFM1前体分子被UFSP1和UFSP2切割,暴露出C端甘氨酸,成为成熟的UFM1。UBA5激活UFM1,通过酯交换反应转移到UFC1。随后,UFL1将UFM1转移到底物蛋白质的赖氨酸残基上。UFBP1和CDK5RAP3是重要的衔接蛋白,辅助UFL1锚定在内质网上,完成对底物的修饰。犹素修饰是可逆的,UFSP2是主要的去修饰酶,与ODR4形成复合物定位在内质网上。犹素系统基因突变与髋关节发育不良及多种神经发育疾病(如,婴儿脑病、小头畸形、共济失调)有关。犹素系统广泛参与调控内质网稳态、基因组稳定性、细胞周期、免疫应答等重要生命过程,对小鼠胚胎发育、浆细胞分化和功能、红细胞分化、肝脏发育、肠道稳态等至关重要。
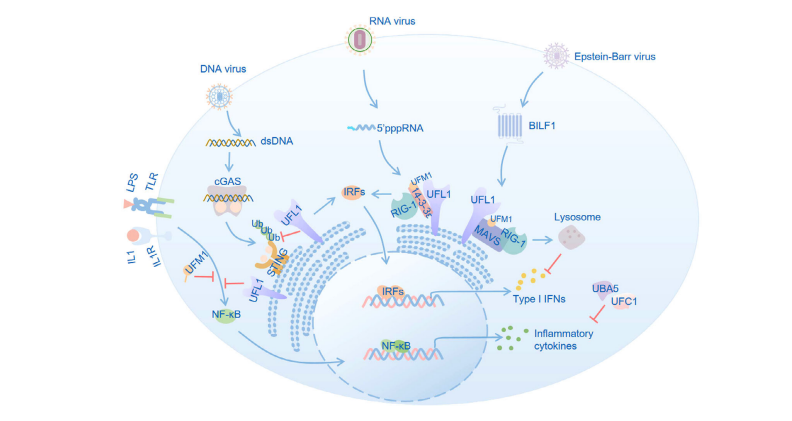
图2.犹素系统对先天免疫的调控作用
犹素系统调控抗病毒免疫和炎症相关信号通路。HSV-1感染时,UFL1与STING结合,抑制其泛素化修饰和蛋白酶体降解。SenV感染时,UFL1与14-3-3ε结合,促进犹素修饰,随后与活化的RIG-1结合,促进下游干扰素的产生。EBV病毒蛋白BILF1与MAVS和UFL1结合,促进MAVS发生犹素修饰,最终导致其进入溶酶体降解。犹素系统抑制IFN-γ或LPS对巨噬细胞的激活,抑制多种炎症因子的产生。
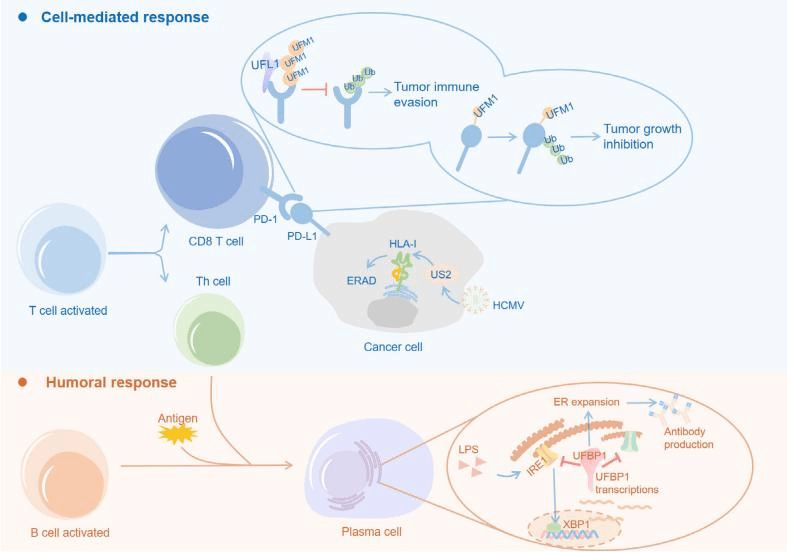
图3. 犹素系统对适应性免疫的调控作用
犹素系统是肿瘤进展的关键调节因子。一方面,UFL1促进PD-L1犹素修饰,促进泛素化修饰和蛋白酶体降解,增强抗肿瘤免疫应答,显著抑制肿瘤生长。另一方面,UFL1促进PD-1犹素修饰,抑制泛素化修饰和蛋白酶体降解,抑制CD8+T细胞的活化。B细胞是执行体液免疫的主要免疫细胞,产生大量特异性抗体。在浆细胞发育过程中,UFBP1抑制PERK通路激活,UFBP1缺失抑制抗体产生。HLA-I类分子可以将抗原提呈给特异性T细胞,UFM1加速HLA-I类分子的内质网相关降解,诱导HCMV病毒免疫逃逸。
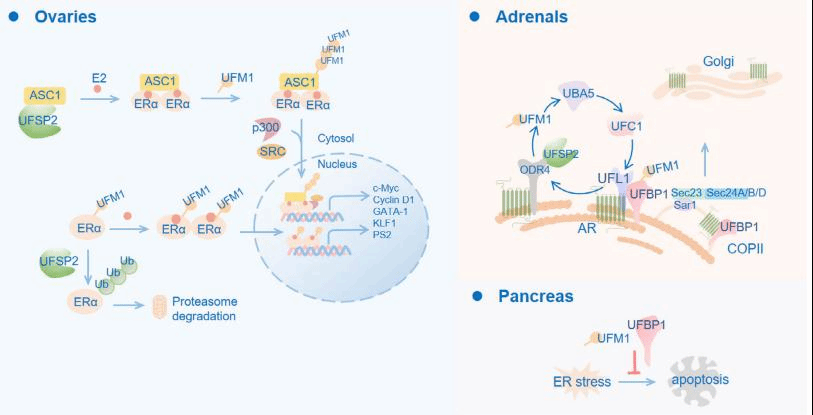
图4.犹素系统对内分泌系统的调控作用
内分泌系统与免疫系统存在密切的相互作用。UFM1缺失破坏肾上腺素受体内质网-高尔基体转运。犹素修饰促进雌激素受体的稳定性和转录活性。犹素系统在胰腺中高表达,保护胰岛β细胞免于内质网应激导致的细胞凋亡。

图5.犹素系统在免疫应答中的调控作用
在适应性免疫应答中,犹素系统调控PD-1/PD-L1免疫检查点和B细胞功能。UFL1促进PD-L1犹素修饰,促进其泛素化修饰和蛋白酶体降解,PD-1抗体联合UFSP2小分子抑制剂显著抑制乳腺癌进展。T细胞中UFL1缺失下调PD-1犹素修饰水平,促进其泛素化修饰和蛋白酶体降解。在浆细胞发育过程中,UFBP1抑制PERK通路的激活,UFBP1缺失抑制浆细胞产生抗体。在先天免疫应答中,犹素系统调控抗病毒免疫和炎症相关信号通路。HSV-1感染时,UFL1与STING结合,抑制其泛素化修饰和蛋白酶体降解。SenV感染时,UFL1与14-3-3ε结合,促进犹素修饰,随后与活化的RIG-1结合,促进下游干扰素的产生。EBV病毒蛋白BILF1介导MAVS的犹素修饰,导致其最终进入溶酶体降解。犹素系统抑制IFN-γ或LPS对巨噬细胞的激活,抑制炎症因子的产生。
简介:
周军智,博士,广东医科大学高层次人才,硕士生导师及博士后合作导师,蛋白修饰与肿瘤微环境研究团队负责人。2014年博士毕业于北京师范大学,从事衰老生物学研究。2014.01至2015.05中国科学院生物物理研究所任职刘光慧课题组助理研究员,从事干细胞衰老的分子机制研究。2015.05至2019.05分别于美国宾夕法尼亚大学医学院、耶鲁大学医学院从事博士后工作,相继开展了肿瘤表观遗传学及肿瘤免疫学研究。2019.05至2024.01在杭州师范大学基础医学院从事蛋白修饰与肿瘤微环境研究。2024.02入职广东医科大学并组建蛋白修饰与肿瘤微环境研究团队。课题组主要研究方向:(1)新型蛋白翻译后修UFMylation在肿瘤微环境中的调控及机制;(2)蛋白UFMylation修饰与肿瘤转移及靶点筛选;(3)新型间充质干细胞衰老调控因子解码。主持项目(在研或已结题):国家自然科学基金面项目(2023立项);广东医科大学高层次人才启动项目(在研);国家自然科学基金青年项目(已结题);2020年高层次留学回国人员在杭创业创新项目;国家重点基础研究发展计划(课题骨干,已结题)。代表作:以第一作者(含共一)或共通讯发表国际性学术论文18篇,代表作包括: 美国科学院院刊PNAS(第一作者及通讯作者);Nature Communications;Aging Cell(老年医学顶刊);Clinical and Translational Medicine(2024);Clinical and Translational Medicine(2021);STAR Protocols(2022,Cell新子刊)。此外,国家发明专利1项。(图、文/周军智 初审/吴洪福 初审/李斯璐 复审/梁志勇 终审/冯明英)